Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (23): 4347-4354.doi: 10.3969/j.issn.2095-4344.2013.23.024
Previous Articles Next Articles
Research and progress in stem cell anti-aging theory
Shan Sha-rui, Huang Guo-zhi
- Department of Rehabilitation, Zhujiang Hospital of Southern Medical University, Guangzhou 510282, Guangdong Province, China
-
Online:2013-06-04Published:2013-06-04 -
Contact:Huang Guo-zhi, Doctoral supervisor, Chief physician, Department of Rehabilitation, Zhujiang Hospital of Southern Medical University, Guangzhou 510282, Guangdong Province, China drhuang66@163.com -
About author:Shan Sha-rui★, Studying for master’s degree, Department of Rehabilitation, Zhujiang Hospital of Southern Medical University, Guangzhou 510282, Guangdong Province, China shansharui@126.com
CLC Number:
Cite this article
Shan Sha-rui, Huang Guo-zhi. Research and progress in stem cell anti-aging theory[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(23): 4347-4354.
share this article
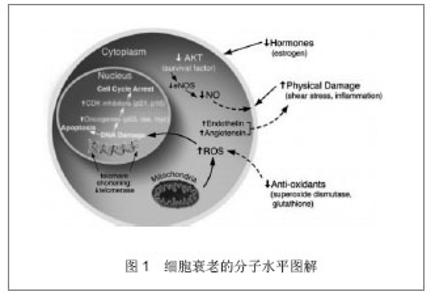
衰老是指在生物发育成熟后,随年龄增加,机体功能减退,内环境稳定能力与应激能力下降,结构、组分逐步退行性变,趋向死亡[10] 。据文献报道单细胞生物如酵母,亦出现衰老倾向,疾病或异常因素可引起病理性衰老,使上述现象提早出现[11] 。伴随着衰老,一些器官的生理功能发生变化甚至会发生病变,如高血压、慢性冠状动脉粥样硬化及糖尿病等,因此衰老是一个重要的研究课题[12] 。本文从衰老标准测定,干细胞定义,干细胞抗衰老研究概况,目前经实验证实有抗衰老作用的几种干细胞及血管内皮祖细胞抗衰老的可能机制方面进行阐述。 2.1 衰老测定标准 关于衰老的几种学说:遗传控制说、自由基损伤说、代谢产物交联说、体细胞突变说、差错积累说、免疫紊乱说、端粒缩短等[13] 。目前较为关注的是基因控制学说(非单基因而是一组基因决定、衰老基因可能是一个基因组) [14-16] ,内外环境环境控制学说(神经、内分泌、免疫系统、体液、激素等)。关于衰老的评定简要从以下方面介绍。 2.1.1 抗氧化物质 1950年Denham Harman提出自由基衰老理论,该学说认为作为细胞代谢产生的一部分自由基,在人体衰老中起很重要的作用,羟基自由基和双氧水对衰老有很大作用[17] 。线粒体产生的细胞内超氧阴离子和双氧水引起衰老。在衰老过程中自由基的产生也与氮氧化物、腺嘌呤、磷酸氧化物、低水平的抗氧化剂有关,例如胞外超氧化物歧化酶,谷胱甘肽过氧化氢酶活力[18] 。超氧化物歧化酶是体内自由基防御体系中最重要的酶类抗氧化剂,它可直接清除超氧阴离子自由基,阻断自由基连锁反应,保护组织免受超氧阴离子自由基的损伤,超氧化物歧化酶活力的高低间接反应机体抗氧化的能力,即反应机体抗衰老能力。具体可见图1[19] 。"
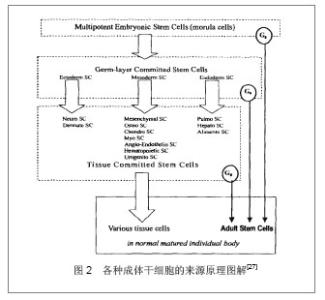
2.1.2 激素类 随着机体衰老,生长激素、甲状腺素、胰岛素样生长因子1等激素浓度降低。Hesse研究表明胰岛素样生长因子1水平与年龄呈负相关,Quevedo等[20]证实了胰岛素样生长因子1通过磷脂酰肌醇-3酶和GSR-3酶介导的eIF-2B对神经元的作用,从而也证实了胰岛素样生长因子1与衰老有关。人类的衰老和血液中的生长激素浓度相关,生长激素调整疗法已经被证实有抗衰老作用[21] 。 2.1.3 免疫系统 Wolford 在20世纪60年代首先提出衰老的免疫学假说,认为免疫系统从根本上参加了正常脊椎动物的衰老过程,是衰老过程的主要调节系统之一。衰老使老年人及实验动物的免疫功能(细胞免疫和体液免疫)下降[22] 。可以通过免疫球蛋白(IgA、IgG、IgM)测定免疫系统机能。 2.1.4 评定量表 胡寒春等编制适合中国中老年人的衰老自评量表(AAS),从衰老生理变化、情绪改变、记忆变化、自我评价的变化、对过往事情的追忆程度、思维灵活性的改变和对将来的期望与态度7个因素进行评价[23] 。另外可以通过以下量表评定机体功能状态:匹兹堡睡眠指数(PSQI)、简明疲劳量表(BFI-C)等。 2.1.5 其他 如机体的心功能、肺功能、骨骼密度等方面,随机体的衰老,心功能及肺功能会改变及降低,骨骼的密度也会下降,机体承受外界压力的能力降低。 2.2 干细胞 2.2.1 干细胞定义 干细胞是具有自我更新能力和多向分化能力的细胞[24] 。按干细胞来源及分化潜能,干细胞可分为全能干细胞和特定组织干细胞(成体干细胞来源于成体组织如脂肪组织、外周血、骨骼、皮肤和肝脏等) [25] 。前者能发育分化形成完整的机体,后者是一种或几种组织的起源细胞。按其分化的差异性分为全能干细胞、多能干细胞、专能干细胞[26] ,图2为成体干细胞来源图解[27"
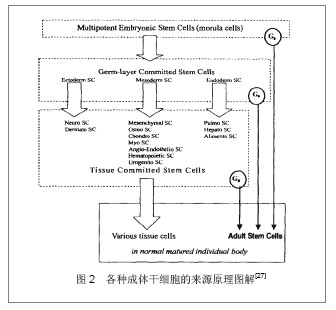

目前,已经从许多组织或器官中成功地分离出干细胞,其中包括:胚胎干细胞、造血干细胞和骨髓间质干细胞等。此外,还有近来研究渐多的神经干细胞、肌肉干细胞、成骨干细胞、内胚层干细胞及视网膜干细胞、血管内皮祖细胞等[28] 。 2.2.2 干细胞抗衰老 在美国《science》杂志评选出的1999年度10大科学进展中,干细胞的研究工作格外令人瞩目。一方面揭示了许多有关细胞生长和发育的基础理论难题;另一方面,干细胞可望将其用于创伤修复、神经再生和抗衰老等临床医学研究。2007年英国科学家 Anastasia 在自然杂志撰文指出成体干细胞对人体自我修复和组织再生至关重要,成体干细胞减少是人体衰老的主要原因[29] 。纤维母细胞、脂肪干细胞及血小板丰富的血浆、培养的真皮乳头细胞在临床已经被成功的用于抗衰老[30] 。 21世纪初,英国西德的尼布伦纳、美国的H罗伯特霍维茨和英国的约翰E苏尔顿3位诺贝尔获得者发现细胞凋亡的规律。人体清除自由基产生抗氧化酶物质,与年龄成负相关,随着年龄增加,抗氧化物质减少,细胞死亡加速[26] 。干细胞内含有几十种促使人体细胞代谢的分化酶,这些分化酶具有提高人体的抗自由基能力。这些活性因子包括超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化氢酶和丰富的核酸、褪黑素、脑腺肽、表皮生长因子、表皮细胞修复因子及多种氨基酸和人体所需要的微量元素,具有维持活细胞和死亡细胞能力数量平衡。 2.3 目前研究的几种抗衰老干细胞 2.3.1 骨髓间充质干细胞 整个生命过程中,当成年人干细胞存在时,组织修复和再生可能进行。骨髓间充质干细胞包括造血干细胞、间叶基质细胞、内皮细胞等,均能对组织进行修复及再生[31] 。 骨髓间充质干细胞能增加血管内皮生长因子等的表达,在大鼠肾脏抗衰老方面起重要作用。骨髓间充质干细胞在衰老组织器官的归巢见图3。成年组织干细胞有助于提高内生细胞再生能力或者转移细胞修复损失及病变组织的能力。大量研究表明成年人干细胞类型和功能特性的变化可能随着年龄的增长有病变发生。特别是氧化代谢应激和慢性抑郁作用增加端粒的消耗及在DNA修复方面的消耗,会引起DNA的破坏和基因的不稳定,导致在复制过程中发生衰老和死亡。修复衰老可以用来预防与衰老相关的紊乱,包括造血免疫紊乱,心力衰竭及心血管病神经功能降低症、肌肉和肠道疾病、动脉粥样硬化及恶性肿瘤等疾病[32] 。"

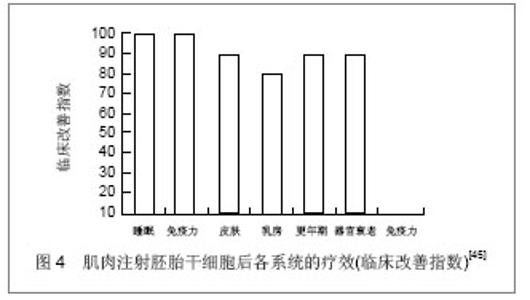
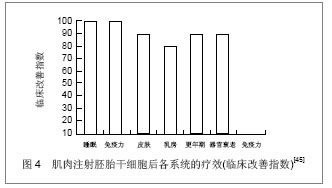
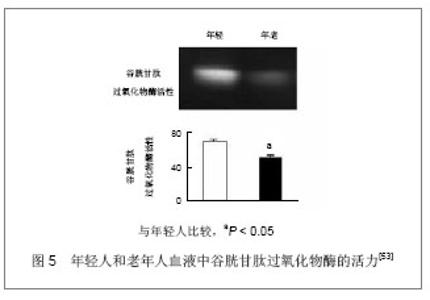
2.3.2 脐血干细胞 1974年 Kandlzon 等首先发现脐血中含有造血祖细胞。随后1982年 Nakahata等发现脐血中的造血祖细胞的产率高于骨髓。Cardoso等[33]比较了骨髓和脐血CD34+ 、CD38-细胞群的分化增殖能力和在长时间培养中产生早期祖细胞的能力。在脐血中CD34+ 、CD38-组分占CD34+群的4%,而在骨髓中只占1%,脐血可能含相对丰富的干细胞。2009年罗利民等以新生儿脐血分离出的间质干细胞,通过尾静脉输入60Co γ射线照射小鼠体内,照射后当天再次输注人脐血间质干细胞,证实脐血间质干细胞静脉输注对辐射造成的脾细胞损伤有一定保护作用,可促进脾脏细胞分裂增殖,加速脾脏细胞修复[34] 。由此可见脐血中干细胞含量较骨髓中丰富,可以成为抗衰老干细胞的一个重要来源。 2.3.3 脂肪干细胞 Zuk等于2001年发现脂肪组织中除了含有已经定型的前脂肪细胞外,也包含一种具有多方向分化潜能的细胞群,其性质与骨髓间充质干细胞相似,这种细胞可以分化成多种组织如骨骼、软骨、脂肪、心肌、神经等组织,同时可以促进伤口愈合、损伤组织细胞再生和减少瘢痕的能力及抗衰老能力[35] 。 杨春等[36]将脂肪源干细胞经尾静脉输入亚急性衰老治疗组大鼠中,结果显示治疗组大鼠血清超氧化物歧化酶、一氧化氮、白细胞介素2水平及脾脏指数均有所提高,而丙二醛含量显著降低。证实异体移植脂肪源干细胞可有效增强大鼠机体清除自由基和抗氧化能力,提高机体免疫功能,延缓D-半乳糖诱发的大鼠衰老。 脂肪干细胞是可以分化成几十种成体干细胞的多能干细胞。多数脂肪干细胞来源于脂肪组织中的纤维组织和血管壁上,少数游离于脂肪间。脂肪来源的干细胞分化能力强,抗衰老效果明显,疗效持久。脂肪干细胞在临床应用中,不仅是填充剂作用,而且可成为永久性再生剂[37-39] 。 2.3.4 生殖干细胞 精子的形成是一个经典的依赖于组织自我更新的特殊组织干细胞。精子干细胞的分化被周围环境的生长因子影响着,用这种干细胞作为抗衰老药,越来越多的认识到干细胞具有维护组织自我更新的能力[40] 。早在1889年,72岁的布朗按照生殖细胞丢失论的学说曾给自己注射狗睾丸的悬浮液,并在一次国际学术大会上作了报告,说他获得了复壮。奥登斯曾用核酸(DNA+RNA)给大白鼠注射,结果使其寿命延长了1倍[41] 。亦有研究认为衰老即是生殖干细胞的丢失,生殖干细胞的补充具有延缓衰老的作用。 2.3.5 胚胎干细胞 20世纪80年代初英国剑桥大学的Evans和Kaufman用延缓着床的胚泡、美国加州大学旧金山分校的Martin用条件培养基分别成功分离、体外培养了小鼠早期胚胎的内团细胞或上胚层细胞,建立了胚胎干细胞系[42-43] 。人胚胎干细胞是多能干细胞的主要来源,研究人员已经通过干细胞培养出血液、内皮、心肌、骨骼、神经细胞。实验证明给衰老小鼠损伤组织植入人胚胎干细胞,胚胎干细胞有固有的抗衰老作用,可以产生可溶性的蛋白,这种物质是MAPK路径中抗衰老的信号。Notch活性激活,或者MAPK通路,TGF信号衰减能唤醒衰老组织的有丝分裂,这种分裂是组织干细胞修复的一个关键部分[44] 。 2002至2004年美国Nebraska大学医学美容整形外科(深圳阳光医疗美容中心)168名人员进行肌肉静脉注射,每周3次,每次1-3 mL,连续4-40 d,研究结果显示受试的对象免疫系统、睡眠、皮肤、乳房、器官衰老、更年期等症状都得到改善[45] ,见图4。证实胚胎干细胞具有抗衰老的作用。但由于伦理学问题,胚胎干细胞应用于临床受限。 "
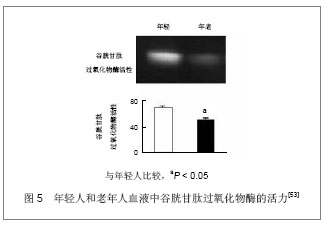
2.4 血管内皮祖细胞临床研究 血管内皮祖细胞应用于治疗缺血性疾病的临床实验已经有十年的历史,近几年,关于血管内皮祖细胞的临床应用研究,文献报道主要应用在急性心肌梗死、难治性心绞痛、肢体缺血、慢性肝病、脑血管病、糖尿病、外周动脉疾病、风湿病及肺动脉高压病等疾病。 1997年,Asahara在Science中报道,人体外周血中分离出表达CD34+和VEGFR-2的细胞,这些细胞能在体外培养分化为内皮细胞,并形成毛细血管样结构[46-47] 。随后人们从骨髓和脐血中分离出血管内皮祖细胞,且证实外周血血管内皮祖细胞来源于骨髓。血管内皮祖细胞是血管内皮细胞的前体,具有迁移特性,能进一步增殖为成熟的内皮细胞。 Aoki等[48]首次应用血管内皮祖细胞在冠状动脉支架上,形成功能内膜覆盖在支架上,然后应用于临床试验,并证明治疗效果优于单纯支架介入治疗。由此可见血管内皮祖细胞可以分化为内皮细胞系,有修复受损内皮细胞[49-50] ,减轻组织缺血、降低高脂血症等对血管内皮的损伤,降低冠心病、肢体缺血等的发病率和致死率,改善组织缺血等提高机体功能。 有研究认为血管内皮祖细胞通过调整血管平滑肌的收缩,调整血流速度和流量,减轻炎症反应,可以提高性功能[51] 。此外据研究,血管内皮祖细胞具有分泌血管内皮生长因子、肝细胞生长因子、胰岛素样生长因子1的能力[52] ,这些因子可对抗机体抗衰老。He等[53]研究老年人血清中血管内皮祖细胞表达的抗自由基产物谷胱甘肽过氧化物酶的量较年轻人血液中血管内皮祖细胞表达的谷胱甘肽过氧化物酶少,见图5。通过以上血管内皮祖细胞的几种临床作用,推测其具有临床抗衰老作用。"
| [1]张建,华琦.我国人口老龄化现状及其应对策略[J].中国健康管理杂志,2009,3(3):135-137.[2]Meeks WM. Pathophysiology of hypertension in the elderly. Semin Nephrol. 2002;22(1):65-70.[3]Stanzione P, Tropepi D. Drugs and clinical trials in neurode- generative diseases. Ann Ist Super Sanita. 2011;47(1):49-54.[4]Baker DJ, Wijshake T, Tchkonia T,et al. Clearance of p16Ink4a-positive senescent cells delays ageing-associated disorders. Nature. 2011;479(7372):232-236.[5]Krishnamurthy J, Torrice C, Ramsey MR, et al. Ink4a/Arf expression is a biomarker of aging. J Clin Invest. 2004; 114(9):1299-1307.[6]Marchand A, Atassi F, Gaaya A, et al. The Wnt/beta-catenin pathway is activated during advanced arterial aging in humans. Aging Cell. 2011;10(2):220-232.[7]Liu S, Liu S, Wang X, et al. The PI3K-Akt pathway inhibits senescence and promotes self-renewal of human skin-derived precursors in vitro. Aging Cell. 2011;10(4): 661-674.[8]Kloet DE, Burgering BM. The PKB/FOXO switch in aging and cancer. Biochim Biophys Acta. 2011;1813(11):1926-1937.[9]Langley E, Pearson M, Faretta M,et al. Human SIR2 deacetylates p53 and antagonizes PML/p53-induced cellular senescence. EMBO J. 2002;21(10):2383-2396.[10]Turnheim K.When drug therapy gets old: pharmacokinetics and pharmacodynamics in the elderly. Exp Gerontol. 2003; 38(8):843-853.[11]Sinclair DA, Lin SJ, Guarente L. Life-span extension in yeast. Science. 2006;312(5771):195-197.[12]Dhahbi JM, Kim HJ, Mote PL, et al. Temporal linkage between the phenotypic and genomic responses to caloric restriction. Proc Natl Acad Sci U S A. 2004;101(15):5524-5529.[13]Xu JX. Differentiation of Constituional Isomer of 2, 2a, 3, 4-Tetrahydro- 4-methyl-2a-phenyl-2-(thiophen-2-yl)- 1H-azeto[2,1-d][ 1,5]benzothiazepin-1-one-5-oxide and Fragmentations of 2,3-Dihydro-2,4-diphenyl-1, 5-benzothiazepine-1-oxide/-1,1-dioxide. Chemical Research in Chinese Universities. 2005;3:274-279.[14]韩晓琳,张宗玉,童坦君.衰老过程中原癌基因及抑癌基因的表达谱[J].生理科学进展, 2002,33(2):126- 130.[15]Zhao L, Tong T, Zhang Z. Expression of the Leo1-like domain of replicative senescence down-regulated Leo1-like (RDL) protein promotes senescence of 2BS fibroblasts. FASEB J. 2005;19(6):521-532.[16]Guo S, Zhang Z, Tong T. Cloning and characterization of cellular senescence-associated genes in human fibroblasts by suppression subtractive hybridization. Exp Cell Res. 2004; 298(2):465-472.[17]Harman D.Aging: a theory based on free radical and radiation chemistry. J Gerontol. 1956;11(3):298-300.[18]Shi Y, Camici GG, Lüscher TF. Cardiovascular determinants of life span. Pflugers Arch. 2010;459(2):315-324.[19]Ballard VL, Edelberg JM. Stem cells and the regeneration of the aging cardiovascular system. Circ Res. 2007;100(8): 1116-1127.[20]Quevedo C, Alcázar A, Salinas M.Two different signal transduction pathways are implicated in the regulation of initiation factor 2B activity in insulin-like growth factor-1-stimulated neuronal cells. J Biol Chem. 2000;275 (25):19192-19197.[21]Lin PC, Chiou TW, Liu PY, et al. Food supplement 20070721-GX may increase CD34+ stem cells and telomerase activity. J Biomed Biotechnol. 2012;2012:498051.[22]Tarazona R, Solana R, Ouyang Q,et al. Basic biology and clinical impact of immunosenescence. Exp Gerontol. 2002; 37(2-3):183-189.[23]胡寒春,邓云龙,范华,等.中老年人衰老自评问卷的初步编制[J].中国临床心理学杂志,2010,18(1):18-20.[24]Weissman IL, Baltimore D. Disappearing stem cells, disappearing science. Science. 2001;292(5517):601.[25]王琪,方向东,戚正武.干细胞的研究进展[J].细胞与分子免疫学杂志,2001,17(1):91-94.[26]张刚庆,方驰华.干细胞研究的问题与对策[J].世界华人消化杂志, 2003,11(12): 2011-2014.[27]唐佩弦. 我国造血干细胞基础研究的新进展兼论干细胞可塑性[J].中国实验血液学杂志, 2003,11(1):1-6.[28]高景恒,袁继龙,王洁晴,等.脂肪来源干细胞与延缓衰老[J].中国美容整形外科杂志, 2011,22(11): 688-691.[29]韩忠朝.干细胞:人类治病健体抗衰老的希望[J].天津科技, 2000 (6):150-165.[30]Ebisawa K, Kagami H, Kato R,et al. Regenerative medicine for anti-aging. Nihon Rinsho. 2009;67(7):1402-1406.[31]李艳菊,胡亮杉,郭坤元. 骨髓间充质干细胞回输对大鼠肾脏衰老的影响[J].中华肾脏病杂志,2009,25(3):241- 242.[32]Li YJ, Deng L, Huang R, et al. The effects of mesenchymal stem cells on the aging kidneys in rats. Zhonghua Nei Ke Za Zhi. 2009;48(6):458-461.[33]Cardoso AA, Li ML, Batard P,et al. Release from quiescence of CD34+ CD38- human umbilical cord blood cells reveals their potentiality to engraft adults. Proc Natl Acad Sci U S A. 1993;90(18):8707-8711.[34]罗利民,布林.静脉输注对60Coγ射线照射小鼠脾脏细胞生物学效应的影响[J].中国组织工程研究与临床康复,2009,13(1): 145-147.[35]李春明,刘毅.脂肪干细胞及其在脂肪组织工程中的应用[J].中国美容医学, 2006,15(4): 466-468.[36]杨春,李东飞,戴景兴,等. 异体脂肪源干细胞移植对大鼠的抗衰老作用[J].解剖学报,2010, 41(1):87-92.[37]Park BS, Jang KA, Sung JH, et al. Adipose-derived stem cells and their secretory factors as a promising therapy for skin aging. Dermatol Surg. 2008;34(10):1323-1326.[38]Song SY, Jung JE, Jeon YR, et al. Determination of adipose- derived stem cell application on photo-aged fibroblasts, based on paracrine function. Cytotherapy. 2011;13(3):378-384.[39]Kim WS, Park BS, Park SH, et al. Antiwrinkle effect of adipose-derived stem cell: activation of dermal fibroblast by secretory factors. J Dermatol Sci. 2009;53(2):96-102.[40]Oatley JM, Brinster RL. The germline stem cell niche unit in mammalian testes. Physiol Rev. 2012;92(2):577-595.[41]刘孟章,李庆昌,衣紫桐,等.生殖干细胞与衰老关系的研究(一)[J].现代中西医结合杂志,2002,11 (13):1231- 1232. [42]Silani V, Fogh I, Ratti A, et al. Stem cells in the treatment of amyotrophic lateral sclerosis (ALS). Amyotroph Lateral Scler Other Motor Neuron Disord. 2002;3(4):173-181.[43]Söderdahl G, Barkholt L, Hentschke P, et al. Liver transplantation followed by adjuvant nonmyeloablative hemopoietic stem cell transplantation for advanced primary liver cancer in humans. Transplantation. 2003;75(7):1061- 1066.[44]Conboy IM, Yousef H, Conboy MJ. Embryonic anti-aging niche. Aging (Albany NY). 2011;3(5):555-563.[45]牛翠霞.胚胎干细胞注射液的临床应用[C].武汉:第八届东南亚地区医学美容学术大会,2004.[46]Asahara T, Murohara T, Sullivan A, et al. Isolation of putative progenitor endothelial cells for angiogenesis.Science. 1997; 275(5302):964-947.[47]Miller-Kasprzak E, Jagodziński PP. Endothelial progenitor cells as a new agent contributing to vascular repair. Arch Immunol Ther Exp (Warsz). 2007;55(4):247-259.[48]Aoki J, Serruys PW, van Beusekom H, et al. Endothelial progenitor cell capture by stents coated with antibody against CD34: the HEALING-FIM (Healthy Endothelial Accelerated Lining Inhibits Neointimal Growth-First In Man) Registry. J Am Coll Cardiol. 2005;45(10):1574-1579.[49]Walter DH, Rittig K, Bahlmann FH,et al. Statin therapy accelerates reendothelialization: a novel effect involving mobilization and incorporation of bone marrow-derived endothelial progenitor cells. Circulation. 2002;105(25): 3017-3024.[50]Kobayashi K, Imanishi T, Akasaka T. Endothelial progenitor cell differentiation and senescence in an angiotensin II-infusion rat model. Hypertens Res. 2006;29(6):449-455.[51]Mikirova NA, Jackson JA, Hunninghake R, et al. Circulating endothelial progenitor cells: a new approach to anti-aging medicine. J Transl Med. 2009;7:106.[52]Klöpper J, Lindenmaier W, Fiedler U, et al. High efficient adenoviral-mediated VEGF and Ang-1 gene delivery into osteogenically differentiated human mesenchymal stem cells. Microvasc Res. 2008;75(1):83-90.[53]He T, Joyner MJ, Katusic ZS. Aging decreases expression and activity of glutathione peroxidase-1 in human endothelial progenitor cells. Microvasc Res. 2009;78(3):447-452. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Xiumei, Zhai Yunkai, Zhao Jie, Zhao Meng. Research hotspots of organoid models in recent 10 years: a search in domestic and foreign databases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1249-1255. |
| [3] | Wang Zhengdong, Huang Na, Chen Jingxian, Zheng Zuobing, Hu Xinyu, Li Mei, Su Xiao, Su Xuesen, Yan Nan. Inhibitory effects of sodium butyrate on microglial activation and expression of inflammatory factors induced by fluorosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1075-1080. |
| [4] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [5] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [6] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [7] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [8] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [9] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [10] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [11] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [12] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [13] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [14] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [15] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||